Recientemente, se aprobó la comercialización de tres medicamentos de terapia génica, a saber: (1) El 21 de julio de 2022, PTC Therapeutics, Inc. (NASDAQ: PTCT) anunció que su terapia génica AAV Upstaza™ fue aprobada por la Comisión Europea. Es la primera terapia génica comercializada inyectada directamente en el cerebro (consulte los artículos anteriores: Otro hito en la terapia génica | Se aprueba la comercialización de la primera terapia génica AAV del mundo inyectada directamente en el cerebro).(2) El 17 de agosto de 2022, la Administración de Alimentos y Medicamentos (FDA) de EE. UU. aprobó la terapia génica Zynteglo (betibeglogene autotemcel, beti-cel) de Bluebird Bio para el tratamiento de la beta talasemia.La aprobación de la terapia en Estados Unidos es sin duda una "ayuda en la nieve" para Bluebird Bio, que se encuentra en crisis financiera.(3) El 24 de agosto de 2022, BioMarin Pharmaceutical (BioMarin) anunció que la Comisión Europea aprobó la comercialización condicional de ROCTAVIAN™ (valoctocogén roxaparvovec), una terapia génica para la hemofilia A, para el tratamiento de pacientes adultos sin antecedentes de inhibidores del factor FVIII y anticuerpos AAV5 negativos con hemofilia A grave (consulte el artículo anterior: Heavy! La terapia génica de la hemofilia A de BioMarin aprobada para su comercialización).Hasta el momento, se han aprobado 41 medicamentos de terapia génica para su comercialización en todo el mundo.
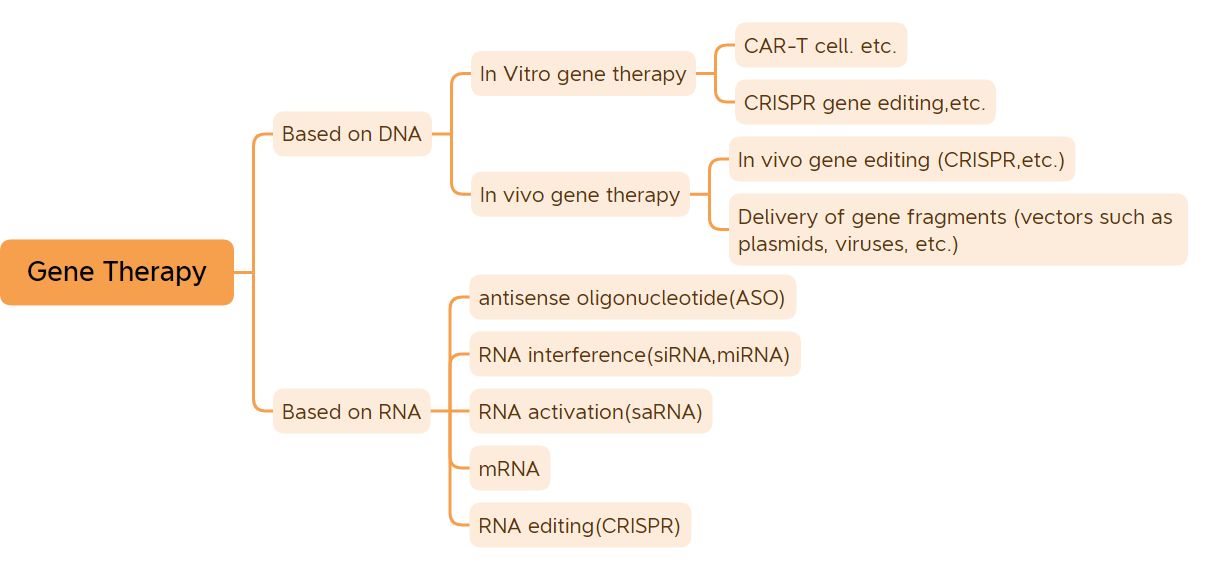
El gen es la unidad genética básica que controla los rasgos.A excepción de los genes de algunos virus, que están compuestos de ARN, los genes de la mayoría de los organismos están compuestos de ADN.La mayoría de las enfermedades del organismo son causadas por la interacción entre los genes y el medio ambiente, y muchas enfermedades pueden curarse o aliviarse esencialmente a través de la terapia génica.La terapia génica se considera una revolución en el campo de la medicina y la farmacia.Los fármacos de terapia génica amplia incluyen fármacos basados en fármacos de ADN modificado con ADN (como fármacos de terapia génica in vivo basados en vectores virales, fármacos de terapia génica in vitro, fármacos de plásmidos desnudos, etc.) y fármacos de ARN (como fármacos de oligonucleótidos antisentido, fármacos de ARNip y terapia génica de ARNm, etc.);En términos estrictos, los medicamentos de terapia génica incluyen principalmente medicamentos de ADN plasmídico, medicamentos de terapia génica basados en vectores virales, medicamentos de terapia génica basados en vectores bacterianos, sistemas de edición de genes y medicamentos de terapia celular modificados genéticamente in vitro.Después de años de desarrollo tortuoso, los medicamentos de terapia génica han logrado resultados clínicos inspiradores.(excluyendo las vacunas de ADN y las vacunas de ARNm), se han aprobado 41 medicamentos de terapia génica para su comercialización en el mundo.Con el lanzamiento de productos y el rápido desarrollo de la tecnología de terapia génica, la terapia génica está a punto de iniciar un período de rápido desarrollo.
Clasificación de la terapia génica (Fuente de la imagen: Biological Jingwei)
Este artículo enumera 41 terapias génicas que han sido aprobadas para su comercialización (excluyendo las vacunas de ADN y las vacunas de ARNm).
1. Terapia génica in vitro
(1) Strimvelis
Empresa: Desarrollado por GlaxoSmithKline (GSK).
Time to market: Aprobado por la Unión Europea en mayo de 2016.
Indicaciones: Para el tratamiento de la inmunodeficiencia combinada severa (SCID).
Observaciones: El proceso general de esta terapia consiste en obtener primero las propias células madre hematopoyéticas del paciente, expandirlas y cultivarlas in vitro, y luego usar retrovirus para introducir una copia del gen funcional ADA (adenosina desaminasa) en sus células madre hematopoyéticas y finalmente transferir las células madre hematopoyéticas modificadas.Las células madre hematopoyéticas se infunden nuevamente en el cuerpo.Los resultados clínicos mostraron que la tasa de supervivencia a 3 años de los pacientes con ADA-SCID tratados con Strimvelis fue del 100 %.
(2) zalmoxis
Compañía: Producido por MolMed, Italia.
Tiempo de comercialización: Obtuvo la autorización de comercialización condicional de la UE en 2016.
Indicaciones: Se utiliza para la terapia adyuvante del sistema inmunitario de pacientes después del trasplante de células madre hematopoyéticas.
Observaciones: Zalmoxis es una inmunoterapia de gen suicida de células T alogénica modificada por un vector retroviral.Los genes suicidas 1NGFR y HSV-TK Mut2 permiten que las personas usen ganciclovir en cualquier momento para matar las células T que causan respuestas inmunitarias adversas, prevenir un mayor deterioro de la EICH que pueda ocurrir y restaurar la función inmunitaria en pacientes con HSCT haploidéntico después de la cirugía Escort.
(3) Invossa-K
Empresa: Desarrollado por la empresa TissueGene (KolonTissueGene).
Tiempo de comercialización: Aprobado para cotizar en Corea del Sur en julio de 2017.
Indicaciones: Para el tratamiento de la artritis degenerativa de rodilla.
Observaciones: Invossa-K es una terapia génica celular alogénica que involucra condrocitos humanos.Las células alogénicas se modifican genéticamente in vitro, y las células modificadas pueden expresar y secretar el factor de crecimiento transformante β1 (TGF-β1) después de la inyección intraarticular.β1), mejorando así los síntomas de la artrosis.Los resultados clínicos muestran que Invossa-K puede mejorar significativamente la artritis de rodilla.La licencia fue revocada por el regulador de medicamentos de Corea del Sur en 2019 porque el fabricante etiquetó incorrectamente los ingredientes utilizados.
(4) Zynteglo
Empresa: Desarrollado por la empresa americana bluebird bio (bluebird bio).
Tiempo de comercialización: Aprobado por la Unión Europea en 2019 y aprobado por la FDA en agosto de 2022.
Indicaciones: Para el tratamiento de la β-talasemia dependiente de transfusiones.
Observaciones: Zynteglo es una terapia génica lentiviral in vitro, que utiliza un vector lentiviral para introducir una copia funcional del gen de la globina β normal (gen de la globina βA-T87Q) en las células madre hematopoyéticas extraídas de los pacientes., y luego infundir estas células madre hematopoyéticas autólogas genéticamente modificadas nuevamente en el paciente.Una vez que el paciente tiene un gen de globina βA-T87Q normal, puede producir una proteína HbAT87Q normal, que puede reducir o eliminar de manera efectiva la necesidad de transfusiones de sangre.Es una terapia única diseñada para reemplazar las transfusiones de sangre de por vida y los medicamentos de por vida para pacientes de 12 años de edad y mayores.
(5) Skysona
Empresa: Desarrollado por la empresa americana bluebird bio (bluebird bio).
Time to market: Aprobado por la UE para su comercialización en julio de 2021.
Indicaciones: Para el tratamiento de la adrenoleucodistrofia cerebral temprana (CALD).
Observaciones: La terapia génica Skysona es la única terapia génica de una sola vez aprobada para el tratamiento de la adrenoleucodistrofia cerebral temprana (CALD).Skysona (elivaldogene autotemcel, Lenti-D) es una terapia génica in vitro lentiviral de células madre hematopoyéticas Lenti-D.El proceso general de la terapia es el siguiente: se extraen células madre hematopoyéticas autólogas del paciente, se modifican in vitro mediante lentivirus que portan el gen ABCD1 humano y luego se infunden de nuevo en el paciente.Para el tratamiento de pacientes menores de 18 años con mutación del gen ABCD1 y CALD.
(6) Quimriah
Empresa: Desarrollado por Novartis.
Tiempo de comercialización: Aprobado por la FDA en agosto de 2017.
Indicaciones: Tratamiento de leucemia linfoblástica aguda (LLA) de células B precursoras y DLBCL recidivante y refractario.
Comentarios: Kymriah es un fármaco de terapia génica in vitro lentiviral, la primera terapia CAR-T aprobada en el mundo, dirigida a CD19 y que utiliza el factor coestimulador 4-1BB.El precio es de $ 475,000 en los EE. UU. y $ 313,000 en Japón.
(7) Yescarta
Empresa: Desarrollado por Kite Pharma, una subsidiaria de Gilead.
Tiempo de comercialización: Aprobado por la FDA en octubre de 2017.
Indicaciones: Para el tratamiento del linfoma de células B grandes en recaída o refractario.
Observaciones: Yescarta es una terapia génica retroviral in vitro.Es la segunda terapia CAR-T aprobada en el mundo.Se dirige a CD19 y utiliza el factor coestimulador de CD28.El precio en los EE. UU. es de $ 373,000.
(8) Tecarto
Empresa: Desarrollado por Gilead (GILD).
Tiempo de comercialización: Aprobado por la FDA en julio de 2020.
Indicaciones: para el linfoma de células del manto en recaída o refractario.
Observaciones: Tecartus es una terapia autóloga de células CAR-T dirigida a CD19, y es la tercera terapia CAR-T aprobada para su comercialización en el mundo.
(9) Breyanzi
Empresa: Desarrollado por Bristol-Myers Squibb (BMS).
Tiempo de comercialización: Aprobado por la FDA en febrero de 2021.
Indicaciones: Linfoma de células B grandes (LBCL) en recaída o refractario (R/R).
Observaciones: Breyanzi es una terapia génica in vitro basada en lentivirus y la cuarta terapia CAR-T aprobada para su comercialización en el mundo, dirigida a CD19.La aprobación de Breyanzi es un hito para Bristol-Myers Squibb en el campo de la inmunoterapia celular, que Bristol-Myers adquirió cuando adquirió Celgene por $74 mil millones en 2019.
(10) Abema
Empresa: Co-desarrollado por Bristol-Myers Squibb (BMS) y bluebird bio.
Tiempo de comercialización: Aprobado por la FDA en marzo de 2021.
Indicaciones: Mieloma múltiple en recaída o refractario.
Observaciones: Abecma es una terapia génica in vitro basada en lentivirus, la primera terapia de células CAR-T del mundo dirigida a BCMA y la quinta terapia CAR-T aprobada por la FDA.El principio del fármaco es expresar el receptor BCMA quimérico en las células T autólogas del paciente a través de la modificación genética in vitro mediada por lentivirus.Antes de la infusión del fármaco del gen celular, el paciente recibió dos compuestos de ciclofosfamida y fludarabina como pretratamiento.Tratamiento para eliminar las células T no modificadas del paciente y luego infundir las células T modificadas nuevamente en el cuerpo del paciente para buscar y eliminar las células cancerosas que expresan BCMA.
(11) Libmeldy
Empresa: Desarrollado por Orchard Therapeutics.
Time to market: Aprobado por la Unión Europea para cotizar en diciembre de 2020.
Indicaciones: Para el tratamiento de la leucodistrofia metacromática (MLD).
Observaciones: Libmeldy es una terapia génica basada en la modificación génica in vitro lentiviral de células CD34+ autólogas.Los datos clínicos muestran que una sola infusión intravenosa de Libmeldy es eficaz para modificar el curso de la MLD de aparición temprana y el deterioro motor y cognitivo grave en pacientes no tratados de la misma edad.
(12) Benoda
Empresa: Desarrollado por WuXi Junuo.
Tiempo de comercialización: Aprobado oficialmente por NMPA en septiembre de 2021.
Indicaciones: Tratamiento del linfoma de células B grandes en recaída o refractario (r/r LBCL) en pacientes adultos después de una terapia de segunda línea o más sistémica.
Observaciones: Benoda es una terapia génica CAR-T anti-CD19 y también es el producto principal de WuXi Junuo.Es el segundo producto CAR-T aprobado en China, excepto para el linfoma de células B grandes en recaída/refractario.Además, WuXi Junuo también planea desarrollar la inyección de Ruiki Orenza para el tratamiento de varias otras indicaciones, incluido el linfoma folicular (FL), el linfoma de células del manto (MCL), la leucemia linfocítica crónica (LLC), el linfoma difuso de células B grandes de segunda línea (DLBCL) y la leucemia linfoblástica aguda (LLA).
(13) CARVYKTI
Empresa: primer producto aprobado de Legend Bio.
Tiempo de comercialización: Aprobado por la FDA en febrero de 2022.
Indicaciones: Tratamiento del mieloma múltiple en recaída o refractario (R/R MM).
Observaciones: CARVYKTI (autoleucel de ciltacabtagén, denominado Cilta-cel) es una terapia génica inmune de células CAR-T con dos anticuerpos de dominio único dirigidos al antígeno de maduración de células B (BCMA).Los datos muestran que CARVYKTI demostró una tasa de respuesta general de hasta el 98 % en pacientes con mieloma múltiple en recaída o refractario que habían recibido cuatro o más tratamientos previos, incluidos inhibidores del proteasoma, inmunomoduladores y anticuerpos monoclonales anti-CD38.
2. Terapia génica in vivo basada en vectores virales
(1) Gendicine/nacido de nuevo
Empresa: Desarrollado por Shenzhen Saibainuo Company.
Tiempo de comercialización: Aprobado para cotizar en China en 2003.
Indicaciones: Para el tratamiento del carcinoma epidermoide de cabeza y cuello.
Observaciones: La inyección de adenovirus p53 humano recombinante Gendicine/Jinshengsheng es un fármaco de terapia génica de vector de adenovirus con derechos de propiedad intelectual independientes propiedad de Shenzhen Saibainuo Company.El fármaco está compuesto por el gen supresor de tumores humano normal p53 y el adenovirus humano tipo 5 de replicación deficiente recombinante modificado artificialmente está compuesto por adenovirus humano tipo 5. El primero es la estructura principal del fármaco para ejercer un efecto antitumoral, y el último actúa principalmente como un vehículo.El vector de adenovirus lleva el gen terapéutico p53 a la célula diana y expresa el gen supresor de tumores p53 en la célula diana.El producto puede regular al alza varios genes anticancerígenos y regular a la baja las actividades de varios oncogenes, mejorando así el efecto antitumoral del cuerpo y logrando el propósito de matar los tumores.
(2) Rigvir
Empresa: Desarrollado por la empresa letona Latima.
Tiempo de comercialización: Aprobado en Letonia en 2004.
Indicaciones: Para el tratamiento del melanoma.
Observaciones: Rigvir es una terapia génica basada en un vector de enterovirus ECHO-7 modificado genéticamente, que se ha utilizado en Letonia, Estonia, Polonia, Armenia, Bielorrusia y otros lugares, y también se está registrando en la EMA de la Unión Europea..Los casos clínicos de los últimos diez años han demostrado que el virus oncolítico Rigvir es seguro y eficaz, y puede mejorar la tasa de supervivencia de los pacientes con melanoma entre 4 y 6 veces.Además, la terapia también es adecuada para una variedad de otros tipos de cáncer, incluido el cáncer colorrectal, el cáncer de páncreas y el cáncer de vejiga.cáncer, cáncer de riñón, cáncer de próstata, cáncer de pulmón, cáncer de útero, linfosarcoma, etc.
(3) Oncorina/Ankerui
Empresa: Desarrollado por Shanghai Sunway Biotechnology Co., Ltd.
Tiempo de comercialización: Aprobado para cotizar en China en 2005.
Indicaciones: Tratamiento de tumores de cabeza y cuello, cáncer de hígado, cáncer de páncreas, cáncer de cuello uterino y otros cánceres.
Observaciones: Oncorine es un producto de terapia génica de virus oncolíticos que utiliza adenovirus como vector.El adenovirus oncolítico obtenido puede replicarse específicamente en tumores que carecen del gen p53 o que son anormales, lo que provoca la lisis de las células tumorales y, por lo tanto, destruye las células tumorales.sin dañar las células normales.Los resultados clínicos muestran que Anke Rui tiene buena seguridad y eficacia para una variedad de tumores malignos.
(4) glybera
Empresa: Desarrollado por uniQure.
Time to market: Aprobado en Europa en 2012.
Indicaciones: Tratamiento de la deficiencia de lipoproteína lipasa (LPLD) con episodios graves o recurrentes de pancreatitis a pesar de una dieta estrictamente restringida en grasas.
Observaciones: Glybera (alipogen tiparvovec) es un fármaco de terapia génica basado en AAV como vector.Esta terapia utiliza AAV como vector para transferir el gen terapéutico LPL a las células musculares, de modo que las células correspondientes puedan producir una cierta cantidad de lipoproteína lipasa. Desempeña un papel en el alivio de la enfermedad, y esta terapia es efectiva durante mucho tiempo después de una administración (el efecto puede durar muchos años).El fármaco se eliminó de la lista en 2017 y los motivos de su eliminación pueden estar relacionados con dos factores: precios demasiado altos y demanda limitada del mercado.El costo promedio de un solo tratamiento del medicamento es de hasta 1 millón de dólares estadounidenses, y hasta ahora solo un paciente lo ha comprado y usado.Aunque la compañía de seguros médicos le reembolsó 900.000 dólares estadounidenses, también es una gran carga para la compañía de seguros.Además, la indicación del fármaco es demasiado rara, con una tasa de incidencia de aproximadamente 1 en 1 millón y una alta tasa de diagnóstico erróneo.
(5) Imlígico
Empresa: Desarrollado por Amgen.
Tiempo de comercialización: en 2015, se aprobó su cotización en los Estados Unidos y la Unión Europea.
Indicaciones: Tratamiento de lesiones de melanoma que no se pueden extirpar completamente mediante cirugía.
Observaciones: Imlygic es un virus oncolítico atenuado del virus del herpes simple tipo 1 (HSV-1) genéticamente modificado (eliminando sus fragmentos de genes ICP34.5 e ICP47 e insertando el gen del factor estimulante de colonias de granulocitos y macrófagos humanos GM-CSF en el virus), la primera terapia génica de virus oncolíticos aprobada por la FDA.El método de administración es inyección intralesional.La inyección directa en las lesiones de melanoma puede provocar la ruptura de las células tumorales y liberar antígenos derivados del tumor y GM-CSF para promover respuestas inmunitarias antitumorales.
(6) Luxturna
Empresa: Desarrollado por Spark Therapeutics, una subsidiaria de Roche.
Tiempo de comercialización: aprobado por la FDA en 2017 y luego aprobado para su comercialización en Europa en 2018.
Indicaciones: Para el tratamiento de niños y adultos con pérdida de visión debida a mutaciones en la copia doble del gen RPE65 pero con un número suficiente de células retinianas viables.
Observaciones: Luxturna es una terapia génica basada en AAV que se administra mediante inyección subretiniana.La terapia génica utiliza AAV2 como portador para introducir una copia funcional del gen RPE65 normal en las células de la retina del paciente, de modo que las células correspondientes expresen la proteína RPE65 normal para compensar el defecto de la proteína RPE65 del paciente, mejorando así la visión del paciente.
(7) Zolgensma
Empresa: Desarrollado por AveXis, una subsidiaria de Novartis.
Tiempo de comercialización: Aprobado por la FDA en mayo de 2019.
Indicaciones: Tratamiento de la atrofia muscular espinal (Atrofia Muscular Espinal, AME) en pacientes menores de 2 años.
Observaciones: Zolgensma es una terapia génica basada en el vector AAV.Este fármaco es el único plan de tratamiento de una sola vez para la atrofia muscular espinal aprobado para su comercialización en el mundo.página, es un hito de progreso.Esta terapia génica utiliza el vector scAAV9 para introducir el gen SMN1 normal en los pacientes a través de una infusión intravenosa, lo que produce la proteína SMN1 normal y, por lo tanto, mejora la función de las células afectadas, como las neuronas motoras.Por el contrario, los medicamentos para la AME Spinraza y Evrysdi requieren dosis repetidas durante un largo período de tiempo, con Spinraza administrado como una inyección espinal cada cuatro meses, y Evrysdi, un fármaco oral diario.
(8) Delytac
Empresa: Desarrollado por Daiichi Sankyo Company Limited (TYO: 4568).
Tiempo de comercialización: Aprobación condicional del Ministerio de Salud, Trabajo y Bienestar de Japón (MHLW) en junio de 2021.
Indicaciones: Para el tratamiento del glioma maligno.
Observaciones: Delytact es el cuarto producto de terapia génica de virus oncolíticos aprobado a nivel mundial y el primer producto de virus oncolíticos aprobado para el tratamiento del glioma maligno.Delytact es un virus oncolítico del virus del herpes simple tipo 1 (HSV-1) modificado genéticamente desarrollado por el Dr. Todo y sus colegas.Delytact introduce una mutación de deleción adicional en el genoma G207 del HSV-1 de segunda generación, mejorando su replicación selectiva en células cancerosas y la inducción de respuestas inmunitarias antitumorales, manteniendo un alto perfil de seguridad.Delytact es el primer oncolítico de tercera generación HSV-1 actualmente en evaluación clínica.La aprobación de Delytact en Japón se basó en un ensayo clínico de fase 2 de un solo grupo.En pacientes con glioblastoma recurrente, Delytact cumplió con el criterio principal de valoración de supervivencia de un año y los resultados mostraron que Delytact funcionó mejor que G207.Fuerte replicación y mayor actividad antitumoral.Esto es efectivo en modelos de tumores sólidos que incluyen tumores de mama, próstata, schwannoma, nasofaríngeo, hepatocelular, colorrectal, tumores malignos de la vaina nerviosa periférica y cáncer de tiroides.
(9) Upstaza
Empresa: Desarrollado por PTC Therapeutics, Inc. (NASDAQ: PTCT).
Time to market: Aprobado por la UE en julio de 2022.
Indicación: Para la deficiencia de L-aminoácido descarboxilasa aromática (AADC), aprobado para el tratamiento de pacientes de 18 meses de edad y mayores.
Observaciones: Upstaza™ (eladocagene exuparvovec) es una terapia génica in vivo que utiliza el virus adenoasociado tipo 2 (AAV2) como vector.El paciente está enfermo debido a una mutación en el gen que codifica la enzima AADC.AAV2 lleva un gen saludable que codifica la enzima AADC.El efecto terapéutico se logra en forma de compensación genética.En teoría, una dosis única es eficaz durante mucho tiempo.Es la primera terapia génica comercializada que se inyecta directamente en el cerebro.La autorización de comercialización es aplicable a los 27 estados miembros de la UE, así como a Islandia, Noruega y Liechtenstein.
(9) Roctaviano
Empresa: Desarrollado por BioMarin Pharmaceutical (BioMarin).
Time to market: Aprobado por la UE en agosto de 2022.
Indicaciones: Para el tratamiento de pacientes adultos con hemofilia A severa sin antecedentes de inhibición del factor FVIII y anticuerpos AAV5 negativos.
Observaciones: Roctavian (valoctocogén roxaparvovec) utiliza AAV5 como vector y utiliza el promotor HLP específico del hígado humano para impulsar la expresión del factor ocho de coagulación humano (FVIII) con el dominio B eliminado.La decisión de la Comisión Europea de aprobar la comercialización de valoctocogén roxaparvovec se basa en los datos generales del programa de desarrollo clínico del fármaco.Entre ellos, el ensayo clínico de fase III GENEr8-1 mostró que, en comparación con los datos del año anterior a la inscripción, después de una infusión única de valoctocogén roxaparvovec, los sujetos tenían una tasa de sangrado anual (ABR) significativamente más baja, un uso menos frecuente de preparaciones de proteína de factor VIII recombinante (F8) o un aumento significativo en la actividad de F8 en la sangre del cuerpo.Después de 4 semanas de tratamiento, el uso anual de F8 y ABR de los sujetos que requerían tratamiento se redujeron en un 99 % y un 84 %, respectivamente, una diferencia estadísticamente significativa (p<0,001).El perfil de seguridad fue favorable, ningún sujeto experimentó inhibición del factor F8, malignidad o efectos secundarios trombóticos, y no se informaron eventos adversos graves (AAG) relacionados con el tratamiento.
3. Fármacos de ácido nucleico pequeño
(1) Vitravene
Empresa: desarrollado conjuntamente por Ionis Pharma (anteriormente Isis Pharma) y Novartis.
Time to market: Aprobado por FDA y EU EMA en 1998 y 1999.
Indicaciones: Para el tratamiento de la retinitis por citomegalovirus en pacientes VIH positivos.
Observaciones: Vitravene es un fármaco oligonucleotídico antisentido y el primer fármaco oligonucleotídico aprobado para su comercialización en el mundo.Al comienzo del mercado, la demanda del mercado de medicamentos contra el citomegalovirus era muy urgente;luego, debido al desarrollo de la terapia antirretroviral altamente activa, el número de casos de citomegalovirus se redujo drásticamente.Debido a la baja demanda del mercado, la droga fue lanzada en 2002 y retirada en 2006 en países de la UE y EE. UU.
(2) macugen
Empresa: Co-desarrollado por Pfizer y Eyetech.
Tiempo de comercialización: Aprobado para cotizar en los Estados Unidos en 2004.
Indicaciones: Para el tratamiento de la degeneración macular asociada a la edad neovascular.
Observaciones: Macugen es un fármaco oligonucleotídico modificado pegilado que puede dirigirse y unirse al factor de crecimiento endotelial vascular (isoforma VEGF165) y se administra mediante inyección intravítrea.
(3) Defitelio
Empresa: Desarrollado por Jazz.
Tiempo de comercialización: Aprobado por la Unión Europea en 2013 y aprobado por la FDA en marzo de 2016.
Indicaciones: Para el tratamiento de la enfermedad oclusiva de las vénulas hepáticas asociada con disfunción renal o pulmonar después de un trasplante de células madre hematopoyéticas.
Observaciones: Defitelio es un medicamento oligonucleótido, una mezcla de oligonucleótidos con propiedades de plasmina.Fue retirado en 2009 por motivos comerciales.
(4) Kynamro
Empresa: Co-desarrollado por Ionis Pharma y Kastle.
Tiempo de comercialización: Aprobado en los Estados Unidos como medicamento huérfano en 2013.
Indicaciones: Para el tratamiento adyuvante de la hipercolesterolemia familiar homocigota.
Observaciones: Kynamro es un fármaco oligonucleótido antisentido, un oligonucleótido antisentido que se dirige al ARNm de apo B-100 humano.Kynamro se administra en dosis de 200 mg por vía subcutánea una vez a la semana.
(5) Espinaza
Empresa: Desarrollado por Ionis Pharmaceuticals.
Tiempo de comercialización: Aprobado por la FDA en diciembre de 2016.
Indicaciones: Para el tratamiento de la atrofia muscular espinal (AME).
Observaciones: Spinraza (nusinersen) es un fármaco oligonucleótido antisentido.Spinraza puede cambiar el empalme del ARN del gen SMN2 al unirse al sitio de empalme del exón 7 de SMN2, lo que aumenta la producción de proteína SMN completamente funcional.En agosto de 2016, BIOGEN Corporation ejerció su opción de adquirir los derechos globales de Spinraza.Spinraza comenzó su primer ensayo clínico en humanos en 2011. En solo 5 años, fue aprobado por la FDA en 2016, lo que refleja el pleno reconocimiento de la FDA sobre su eficacia.El medicamento fue aprobado para su comercialización en China en abril de 2019. El ciclo completo de aprobación de Spinraza en China es de menos de 6 meses.Han pasado 2 años y 2 meses desde que Spinraza fue aprobado por primera vez en los Estados Unidos.Un nuevo fármaco extranjero para enfermedades raras de gran éxito está en La velocidad de cotización en China ya es muy rápida.Esto también se debe al "Aviso sobre la publicación de la primera lista de nuevos medicamentos extranjeros que se necesitan con urgencia para la investigación clínica" emitido por el Centro de Evaluación de Medicamentos el 1 de noviembre de 2018, que se incluyó en el primer lote de 40 nuevos medicamentos extranjeros clave para revisión acelerada, y Spinraza se clasificó.
(6) Exondis 51
Empresa: Desarrollado por AVI BioPharma (posteriormente rebautizada como Sarepta Therapeutics).
Tiempo de comercialización: Aprobado por la FDA en septiembre de 2016.
Indicaciones: Para el tratamiento de la distrofia muscular de Duchenne (DMD) con mutación del gen DMD en el gen de omisión del exón 51.
Observaciones: Exondys 51 es un fármaco de oligonucleótidos antisentido.El oligonucleótido antisentido puede unirse a la posición del exón 51 del pre-ARNm del gen DMD, dando como resultado la formación de ARNm maduro.La escisión, corrigiendo así parcialmente el marco de lectura del ARNm, ayuda al paciente a sintetizar algunas formas funcionales de distrofina que son más cortas que la proteína normal, mejorando así los síntomas del paciente.
(7) Tegsedi
Empresa: Desarrollado por Ionis Pharmaceuticals.
Time to market: Aprobado por la Unión Europea para su comercialización en julio de 2018.
Indicaciones: Para el tratamiento de la amiloidosis hereditaria por transtiretina (hATTR).
Observaciones: Tegsedi es un fármaco oligonucleótido antisentido que se dirige al ARNm de la transtiretina.Es el primer fármaco aprobado en el mundo para el tratamiento de hATTR.El método de administración es inyección subcutánea.El fármaco reduce la producción de la proteína ATTR al dirigirse al ARNm de la transtiretina (ATTR) y tiene una buena relación riesgo-beneficio en el tratamiento de la ATTR.Ni el estadio de la enfermedad ni la presencia de miocardiopatía fueron relevantes.
(8) En patro
Empresa: Co-desarrollado por Alnylam y Sanofi.
Tiempo de comercialización: Aprobado para cotizar en los Estados Unidos en 2018.
Indicaciones: Para el tratamiento de la amiloidosis hereditaria por transtiretina (hATTR).
Observaciones: Onpattro es un fármaco de ARNsi que se dirige al ARNm de la transtiretina, que reduce la producción de la proteína ATTR en el hígado y la acumulación de depósitos de amiloide en los nervios periféricos al atacar el ARNm de la transtiretina (ATTR)., mejorando y aliviando así los síntomas de la enfermedad.
(9) Givlaari
Empresa: Desarrollado por Alnylam Corporation.
Tiempo de comercialización: Aprobado por la FDA en noviembre de 2019.
Indicaciones: Para el tratamiento de la porfiria hepática aguda (AHP) en adultos.
Observaciones: Givlaari es un fármaco de ARNip, el segundo fármaco de ARNip aprobado para su comercialización después de Onpattro.El fármaco se administra por vía subcutánea y se dirige al ARNm para la degradación de la proteína ALAS1.El tratamiento mensual con Givlaari puede reducir significativa y persistentemente el nivel de ALAS1 en el hígado, lo que reduce los niveles de ALA y PBG neurotóxicos al rango normal y, por lo tanto, alivia los síntomas de la enfermedad del paciente.Los datos mostraron que los pacientes tratados con Givlaari tuvieron una reducción del 74 % en el número de brotes de la enfermedad en comparación con el grupo de placebo.
(10) Vyondys53
Empresa: Desarrollado por Sarepta Therapeutics.
Tiempo de comercialización: Aprobado por la FDA en diciembre de 2019.
Indicación: Para el tratamiento de pacientes con DMD con mutación de empalme del exón 53 del gen de la distrofina.
Observaciones: Vyondys 53 es un fármaco de oligonucleótidos antisentido.El fármaco oligonucleótido se dirige al proceso de empalme del precursor de ARNm de distrofina.En el proceso indirecto del precursor de ARNm de distrofina, el exón 53 externo se empalmó parcialmente, es decir, no estaba presente en el ARNm maduro, y se diseñó para producir una proteína distrofina truncada pero aún funcional, mejorando así la capacidad de ejercicio en los pacientes.
(11) Waylívra
Empresa: Desarrollado por Ionis Pharmaceuticals y su subsidiaria Akcea Therapeutics.
Time to market: Aprobado por la Agencia Europea de Medicamentos (EMA) en mayo de 2019.
Indicación: Como terapia adjunta a una dieta controlada en pacientes adultos con síndrome de quilomicronemia familiar (FCS).
Observaciones: Waylivra es un fármaco de oligonucleótidos antisentido, que es el primer fármaco aprobado para el tratamiento de FCS en el mundo.
(12) Leqvio
Empresa: Desarrollado por Novartis.
Time to market: Aprobado por la UE en diciembre de 2020.
Indicaciones: Para el tratamiento de la hipercolesterolemia primaria del adulto (familiar heterocigota y no familiar) o dislipidemia mixta.
Observaciones: Leqvio es un fármaco de ARNip dirigido al ARNm de PCSK9.Es la primera terapia de ARNip para reducir el colesterol (LDL-C) del mundo.El método de administración es inyección subcutánea.El fármaco funciona mediante la interferencia del ARN para reducir los niveles de proteína PCSK9, lo que a su vez reduce los niveles de LDL-C.Los datos clínicos muestran que Leqvio puede reducir el C-LDL en aproximadamente un 50 % en pacientes cuyos niveles de C-LDL no pueden reducirse a los niveles objetivo a pesar de las dosis máximas toleradas de estatinas.
(13) Oxlumo
Empresa: Desarrollado por Alnylam Pharmaceuticals.
Time to market: Aprobado por la UE en noviembre de 2020.
Indicaciones: Para el tratamiento de la hiperoxaluria primaria tipo 1 (PH1).
Observaciones: Oxlumo es un fármaco de ARNip dirigido al ARNm de la hidroxiácido oxidasa 1 (HAO1), que se administra por vía subcutánea.El fármaco se desarrolló utilizando la última tecnología de conjugación ESC-GalNAc química de estabilización mejorada de Alnylam, que permite la administración subcutánea de siRNA con mayor persistencia y eficacia.El fármaco se dirige a la degradación o inhibición del ARNm de la hidroxiácido oxidasa 1 (HAO1), reduce el nivel de glicolato oxidasa en el hígado y luego consume el sustrato necesario para la producción de oxalato y reduce la producción de oxalato para controlar la progresión de la enfermedad y mejorar los síntomas de la enfermedad en los pacientes.
(14) Viltepso
Empresa: Desarrollado por NS Pharma, una subsidiaria de Nippon Shinyaku.
Tiempo de comercialización: Aprobado por la FDA en agosto de 2020.
Indicaciones: Para el tratamiento de la distrofia muscular de Duchenne (DMD) con mutación del gen DMD en el gen de omisión del exón 53.
Observaciones: Viltepso es un fármaco oligonucleótido de fosforodiamida morfolino.Este fármaco oligonucleótido puede unirse a la posición del exón 53 del pre-ARNm del gen DMD, lo que da como resultado la formación de ARNm maduro.El exón se elimina parcialmente, lo que corrige parcialmente el marco de lectura del ARNm, lo que ayuda al paciente a sintetizar algunas formas funcionales de distrofina que son más cortas que la proteína normal, lo que mejora los síntomas del paciente.
(15) Amvuttra (vutrisirán)
Empresa: Desarrollado por Alnylam Pharmaceuticals.
Tiempo de comercialización: Aprobado por la FDA en junio de 2022.
Indicaciones: Para el tratamiento de la amiloidosis hereditaria por transtiretina en adultos con polineuropatía (hATTR-PN).
Observaciones: Amvuttra (Vutrisiran) es un fármaco de ARNip dirigido al ARNm de la transtiretina (ATTR), que se administra mediante inyección subcutánea.Vutrisiran está diseñado en base a la plataforma de administración conjugada GalNAc de química de estabilización mejorada (ESC) de Alnylam con mayor potencia y estabilidad metabólica.La aprobación de la terapia se basa en datos de 9 meses de su estudio clínico de Fase III (HELIOS-A), con resultados generales que muestran que la terapia mejoró los síntomas de hATTR-PN, con más del 50% de los pacientes revirtiendo o deteniendo la progresión.
4. Otros fármacos de terapia génica
(1) Rexin-G
Empresa: Desarrollado por Epeius Biotech.
Tiempo de comercialización: Aprobado por la Administración de Alimentos y Medicamentos de Filipinas (BFAD) en 2005.
Indicaciones: Para el tratamiento de cánceres avanzados que son resistentes a la quimioterapia.
Observaciones: Rexin-G es una inyección de nanopartículas cargadas de genes.Introduce el gen mutante de la ciclina G1 en las células diana a través de un vector retroviral para eliminar específicamente los tumores sólidos.El método de administración es la infusión intravenosa.Como un fármaco dirigido al tumor que busca y destruye activamente las células cancerosas metastásicas, tiene cierto efecto en los pacientes que son ineficaces frente a otros fármacos contra el cáncer, incluidos los productos biológicos dirigidos.
(2) neovascularización
Empresa: Desarrollado por el instituto de células madre humanas.
Tiempo de listado: Aprobado para cotizar en Rusia el 7 de diciembre de 2011 y luego listado en Ucrania en 2013.
Indicaciones: Para el tratamiento de la enfermedad arterial periférica, incluida la isquemia grave de las extremidades.
Observaciones: Neovasculgen es una terapia génica basada en plásmidos de ADN en la que el gen del factor de crecimiento endotelial vascular (VEGF) 165 se construye en un esqueleto de plásmido y se infunde en los pacientes.
(3) Colategene
Empresa: Co-desarrollado por la Universidad de Osaka y firmas de capital de riesgo.
Tiempo de cotización: Aprobado por el Ministerio de Salud, Trabajo y Bienestar de Japón para cotización en agosto de 2019.
Indicaciones: Tratamiento de la isquemia grave de las extremidades inferiores.
Observaciones: Collategene es una terapia génica basada en plásmidos, el primer fármaco de terapia génica nativo japonés producido por AnGes.El componente principal de este fármaco es un plásmido desnudo que contiene la secuencia del gen del factor de crecimiento de hepatocitos humanos (HGF).Si el fármaco se inyecta en los músculos de las extremidades inferiores, el HGF expresado promoverá la formación de nuevos vasos sanguíneos alrededor de los vasos sanguíneos ocluidos.Los ensayos clínicos han confirmado su eficacia para mejorar las úlceras.
FIN
Hora de publicación: 10-nov-2022